Samenvatting
Wanrooij BS, Koelewijn M. Verlichting van dyspnoe in de palliatieve fase. Huisarts Wet 2005;48(5):239-45. In dit artikel belichten wij de begeleiding van oncologische patiënten met dyspnoe. Dyspnoe komt veel voor in de palliatieve fase van hartfalen, COPD en kanker. Het aantal patiënten hiermee zal de komende jaren aanzienlijk toenemen. Dyspnoe heeft grote invloed op de kwaliteit van leven en gaat bijna altijd gepaard met angst. Ernstige benauwdheid is niet alleen voor de patiënt en zijn naasten, maar vaak ook voor de hulpverlener een angstige ervaring. Dyspnoe kan veel oorzaken hebben die vaak naast elkaar voorkomen. Kennis van het beloop van de onderliggende aandoening en van pathofysiologische achtergronden is nuttig om de mogelijke oorzaak te kunnen achterhalen. Veel causale behandelingen vinden in overleg met de specialist in het ziekenhuis plaats, afhankelijk van de conditie, prognose en wens van de patiënt. De symptomatische aanpak is gericht op het verlichten van de dyspnoe, op de beleving en de gevolgen hiervan. Morfine speelt hierbij een belangrijke rol. De begeleiding gebeurt in nauwe samenwerking met wijkverpleegkundige en fysiotherapeut.
Serie Palliatieve zorg
In een reeks van acht artikelen geven we een breed overzicht van de mogelijkheden van huisartsgeneeskundige zorg voor patiënten in de palliatieve fase. In de vorige afleveringen is aandacht besteed aan basisprincipes van palliatieve zorg, pijn en misselijkheid en braken. In dit vierde artikel gaan we in op dyspnoe. In de volgende artikelen behandelen we samenwerking in de palliatieve zorg, delier, depressie en palliatieve sedatie.
Inleiding
Iedere huisarts-in-opleiding woont een conferentie bij over astma en COPD. Vroeger voerden de deelnemers in een van de sessies de volgende korte oefening uit om te voelen wat het is om benauwd te zijn: adem door een rietje en maak 10 diepe kniebuigingen. Het effect was indrukwekkend. Iedereen was opgelucht als hij, snakkend naar lucht en met een gevoel van lichte paniek, het rietje weer uit zijn mond mocht nemen. Deze oefening was bedoeld, en ook effectief, om benauwdheid te beleven en daardoor een patiënt beter te begrijpen. Toch kan bijna iedereen zich ook zonder zo'n oefening voorstellen dat het afschuwelijk is om ernstig benauwd te zijn; het zien alleen al van een patiënt die erg kortademig is, kan ook bij omstanders gevoelens van benauwdheid en angst veroorzaken. Een veel gebruikte definitie van dyspnoe is: een onaangename subjectieve gewaarwording meer te moeten ademen en/of meer moeite te hebben met ademen. Patiënten gebruiken verschillende uitdrukkingen om aan te geven dat ze een tekort aan lucht hebben, naar adem snakken, moe zijn, kortademig zijn, snel achter de adem zijn, het benauwd hebben, het gevoel hebben te zullen stikken of bang zijn te zullen stikken. In deze uitdrukkingen komt naast de fysieke beleving ook sterk de emotionele beleving naar voren. Benauwdheid of dyspnoe is, net als pijn, niet objectief in maat en getal uit te drukken: een patiënt is zo benauwd als hij zelf aangeeft dat hij is.
De kern
- Het aantal patiënten met dyspnoe als gevolg van hartfalen, COPD en kanker neemt de komende jaren aanzienlijk toe.
- Dyspnoe en angst zijn bijna onlosmakelijk met elkaar verbonden en verdienen beide aandacht bij de behandeling.
- Er zijn verschillende mogelijkheden om dyspnoe causaal te behandelen en daardoor de kwaliteit van leven te verbeteren.
- Veel causale behandelingen kunnen alleen in het ziekenhuis uitgevoerd worden.
- Bij de symptomatische aanpak is morfine het middel bij uitstek.
- Zuurstoftoediening, psychologische ondersteuning en fysiotherapeutische begeleiding kunnen bijdragen aan verdere verlichting van de symptomen en verbetering van de kwaliteit van leven.
Ademen is nodig om te leven, om te communiceren met anderen, om zich uit te drukken in zang en bij sporten bijvoorbeeld. Een tekort aan adem geeft dan ook op veel niveaus van leven beperkingen. Patiënten zijn moe omdat ze benauwd zijn, maar ook omdat ze daardoor nogal eens slecht slapen. De acute verergeringen van de dyspnoe, die optreden onder invloed van inspanning of emoties, veroorzaken angst en paniek. De patiënt is fysiek sterk beperkt in zijn bezigheden binnenshuis en daarbuiten. Dit heeft invloed op het sociale leven en taken in huis. Het besef dat ook patiënten met hartfalen en COPD palliatieve zorg nodig hebben, is de laatste jaren duidelijk toegenomen. Dit heeft een positieve invloed op de kwaliteit van leven van deze groep patiënten. In dit artikel besteden we aandacht aan vóórkomen, oorzaken en behandeling van dyspnoe bij kankerpatiënten in de palliatieve fase. Wij gebruiken hier de termen dyspnoe en benauwdheid door elkaar. De specifieke behandeling van dyspnoe bij COPD en hartfalen valt buiten het bestek van dit artikel.
Mevrouw Vrede
Mevrouw Vrede is 74 jaar en woont zelfstandig. Zij is een kleine, fragiele vrouw. Haar man is 3 jaar geleden overleden. Zij heeft geen kinderen, maar heeft veel contact met haar familie. De huisarts ziet haar regelmatig in verband met haar hoge bloeddruk. Sinds haar 18e jaar rookt zij anderhalf pakje sigaretten per dag. Op een gegeven moment kwam zij tussen de controles door op het spreekuur wegens vermoeidheid en toenemende kortademigheid bij fietsen en traplopen. Zij was afgevallen en had gemerkt dat haar gezicht en haar rechter arm dikker waren geworden en haar rechter ooglid lager hing. Deze klachten waren in een periode van ongeveer zes weken ontstaan en bleken te berusten op een vena-cava-superiorsyndroom (VCS-syndroom), veroorzaakt door een grootcellig longcarcinoom rechts, stadium T3N2M0. Zij had daarbij een syndroom van Horner. Mevrouw Vrede werd bestraald, waarop haar conditie iets verbeterde. Een paar weken later moest zij opgenomen worden wegens vermoeidheid en dyspnoe. Ondanks de bestraling was de tumor verder gegroeid, waardoor de rechter hoofdbronchus nu volledig afgesloten was. Er waren geen therapeutische opties meer. Toen de huisarts haar in het ziekenhuis bezocht, sprak hij met haar over haar slechte prognose. Omdat zij graag naar huis wilde, werden thuiszorg en naaste familie ingeschakeld. Dit kon op zeer korte termijn geregeld worden. De huisarts bezocht haar thuis na ontslag. Mevrouw Vrede was erg verdrietig over het snelle beloop van haar ziekte en kon het duidelijk nog niet allemaal bevatten. De benauwdheid was haar voornaamste probleem. Zij gebruikte daarvoor tweemaal daags 10 mg langwerkende morfine, waarmee de klachten dragelijk waren. Dat betekende wel dat zij bijna voortdurend in bed lag.
Vóórkomen
Dyspnoe hoort tot de meest voorkomende symptomen in de laatste fase van veel chronische en uiteindelijk dodelijke ziekten zoals kanker, terminaal hartfalen en COPD. De prevalentie van dyspnoe is al hoog vanaf een halfjaar voor het overlijden. Zo heeft 78% van de patiënten met longkanker, 88% van de patiënten met hartfalen en 96% van de patiënten met COPD gedurende de laatste 6 maanden van het leven last van dyspnoe. 1 Bij neurologische aandoeningen als ALS en dementie is dyspnoe vooral in de laatste weken een groot probleem. 2 Bij tweederde van de patiënten met dementie komt dyspnoe voor in de laatste fase van het leven. Dyspnoe komt, behalve bij longkanker, ook vaak voor bij andere vormen van kanker. De prevalentie in de hele groep ligt rond 50%. In de laatste 6 weken van het leven klaagt 70% over dyspnoe. Bijna 30% van de patiënten omschrijft deze klachten als matig tot ernstig. 3 In de komende jaren zullen steeds meer mensen aandoeningen krijgen die gepaard gaan met dyspnoe. Betere behandelmogelijkheden van het hartinfarct bijvoorbeeld, veroorzaken een toename van het aantal patiënten met hartfalen en dus met dyspnoe. 4
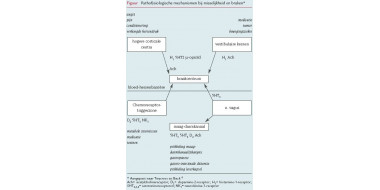
De regulatie van de ademhaling
Lucht wordt ingeademd door neus en mond en komt via de trachea en de bronchi terecht in de alveoli. Diepte en frequentie van de ademhaling veranderen met de eisen die op elk moment aan het lichaam gesteld worden. De regulatie van de ademhaling is complex en is op een sterk vereenvoudigde manier als volgt te beschrijven. 3,5 Centra in de medulla ontvangen signalen van perifere en centrale chemoreceptoren (hypoxie, hypercapnie, veranderingen in de pH van de cerebrospinale vloeistof), van mechanoreceptoren in de ademhalingsspieren (spierzwakte, rek), luchtwegen en longen (longoedeem) en van hogere corticale centra (angst). Deze informatie beïnvloedt frequentie en diepte van de ademhaling. Het gevoel van dyspnoe zou ontstaan wanneer er een discrepantie bestaat tussen afferente informatie en de activiteit van de ademhalingsspieren. Overigens zijn diepte en frequentie van ademhaling ook bewust vanuit de corticale centra te regelen.
Oorzaken
Zoals aangegeven in het vorige hoofdstuk werken vele systemen op elkaar in om de ademhaling te reguleren. Bij het ontstaan van dyspnoe spelen dan ook bijna altijd meerdere factoren een rol. De oorzaken van dyspnoe bij patiënten in de palliatieve fase zijn in te delen naar de lokalisatie van het probleem: luchtwegen, longen, thoraxwand, buiten de thorax gelegen en in het cardiovasculaire systeem. Dyspnoe kan ook een psychologische oorsprong hebben. Op deze wijze is weer een verdere onderverdeling te maken zoals beschreven is in de tabel.
| Lokalisatie | Oorzaken |
|---|---|
| Hogere luchtwegen | obstructie mond/neus/keelholte of trachea door tumor, sputum of secreet |
| Lagere luchtwegen | bronchusobstructie door ingroeiende tumor, astma/COPD |
| Longen | infectie, tumor of metastase, gevolgen van behandeling, pleuritis carcinomatosa, hemoptoë/bloeding, pneumothorax, lymfangitis carcinomatosa |
| Cardiovasculair | decompensatio cordis, anemie, longembolie, vena-cava-superiorsyndroom, pericarditis carcinomatosa |
| Thoraxwand | spierslapte, excursiebeperking, verlamming diafragma |
| Buiten de thorax | ascites, vergrote lever |
| Psychisch | angst, hyperventilatie, depressie |
Pathofysiologische achtergronden
Gedeeltelijke of totale obstructie van de luchtwegen ontstaat door ingroei van tumorweefsel in de trachea of bronchus bij longcarcinoom of metastasen van elders. Obstructie kan ook optreden bij uitbreiding van de tumor naar de hilus of het mediastinum. De mate van dyspnoe is afhankelijk van de lokalisatie van het probleem: hoe hoger gelegen, hoe meer problemen tot zelfs (dreigende) verstikking toe. Dit laatste kan vrij acuut optreden wanneer in de tumor een bloeding ontstaat. Het is overigens opmerkelijk dat patiënten met een vernauwing van de hoofdbronchus tot wel 60% zich vaak ernstiger benauwd voelen dan wanneer deze bronchus totaal is afgesloten. Hemoptoë kan een eerste teken zijn van een longcarcinoom. In de palliatieve fase treedt dit op bij ongeveer de helft van deze groep patiënten. 6 Nogal eens wordt 200 ml tot 1 liter bloed per dag opgegeven of opgehoest. De dyspnoe ontstaat vooral door het bloed dat achterblijft in de longen. Bij ongeveer 3% van de patiënten met primair longcarcinoom treedt een massale longbloeding op die gepaard gaat met zeer ernstige dyspnoe, letterlijke doodsnood en uiteindelijk overlijden. Bij een volledige afsluiting van een van de grotere bronchiën kan atelectase van het daarachter liggend gedeelte optreden, zodat dit uitgeschakeld is bij de ventilatie. In dit soort situaties kunnen patiënten moeilijk sputum ophoesten. Er ontstaan makkelijker infecties, waardoor de dyspnoe verder toeneemt. Een toename van pleuravocht komt voor bij hartfalen en bij meer dan de helft van de patiënten met gemetastaseerde maligniteit. Er is een disbalans tussen de productie en de opname van het pleuravocht ten gevolge van pleurale metastasen, doorgroei in de thoraxwand of belemmerde afvloed. Dit probleem doet zich vooral voor bij longtumoren en metastasen van met name mammacarcinoom. 7 Er zijn nog meer veelvoorkomende complicaties bij bronchus- en mammacarcinoom die dyspnoe teweeg kunnen brengen. Zo leidt lymfangitis carcinomatosa tot diffuse infiltratie en obstructie van de lymfvaten in de longen, hetgeen de gasuitwisseling verstoort. Pericarditis carcinomatosa veroorzaakt vochtophoping in het pericard. Dit heeft een negatief effect op de pompfunctie van het hart. Een longembolie komt bij ongeveer 10% van de patiënten met gemetastaseerde ziekte voor. 8 Een massale embolie kan een acute dood veroorzaken. Een kleine embolie sluit een kleinere vene af waardoor het oppervlakte voor gasuitwisseling afneemt. Dit veroorzaakt nogal eens kortdurend dyspnoe. Als er sprake is van meerdere kleine embolieën, zijn de klachten ernstiger. Ascites of een vergrote lever drukken de longen omhoog, waardoor deze minder kunnen expanderen. Beschadiging van de n. phrenicus ten gevolge van tumoringroei veroorzaakt diafragmaparalyse, waardoor de long aan de aangedane kant niet voldoende kan uitzetten.
Mevrouw Vrede (vervolg)
De zorg voor mevrouw Vrede was goed geregeld. Enkele nichtjes wisselden elkaar hierbij af. De thuiszorg kwam regelmatig langs. In het ziekenhuis had mevrouw Vrede zuurstof toegediend gekregen. Zij vertelde dat dit haar klachten verlichtte. Hierop besloot de huisarts ook thuis zuurstof te regelen. Van de medicatie werd alleen eenmaal daags 12,5 mg hydrochloorthiazide gecontinueerd. Zij gebruikte verder eenmaal daags 4 mg dexamethason vanwege het VCS-syndroom en éénmaal daags een sachet macrogol/elektrolyten in verband met het morfinegebruik.
Mevrouw Vrede was angstig. Deze angst nam enorm toe in de periodes dat de benauwdheid veel erger was. De familie of de wijkverpleegkundige nam haar op zo'n moment in de armen om dicht bij haar te zijn en haar te ondersteunen. Omdat zij steeds angstiger werd, stemde zij toe hiervoor driemaal daags 10 mg oxazepam te gaan gebruiken. Dit verlichtte de angst. De morfine werd geleidelijk opgehoogd. In een gesprek met de huisarts vertelde zij dat zij bang was om te stikken. De uitleg over de mogelijkheden die er zijn om dit te voorkomen, gaf meer rust. De dyspnoe nam toe en de toestand van mevrouw Vrede verslechterde snel. Omdat slikken steeds moeilijker ging, kreeg zij een subcutane pomp. Met een uiteindelijke dosering van 30 mg morfine per 24 uur en driemaal daags 10 mg diazepam rectioles was zij weliswaar wat suf, maar kon zij de benauwdheid veel beter verdragen. Binnen 14 dagen na ontslag uit het ziekenhuis is mevrouw vrij rustig overleden.
Anticiperen
Ook bij dyspnoe is anticiperen zinvol om de patiënt goed te kunnen begeleiden en soms erger leed te voorkomen. Er zijn verschillende palliatieve behandelmogelijkheden voor het geval een bronchus dreigt af te sluiten, zoals bestraling of laserbehandeling. Bij mevrouw Vrede groeide de tumor door ondanks de bestraling, zodat een volledige afsluiting optrad. De huisarts kan met de patiënt en zijn naasten van tevoren bespreken wat de mogelijkheden zijn als de patiënt in de laatste fase van de ziekte een pneumonie zou krijgen. De keuze voor een oorzakelijke behandeling met de complicaties die daarbij kunnen optreden wordt afgezet tegen maximaal symptomatisch behandelen om de patiënt een mogelijk milde dood niet te onthouden. Afspraken hierover dienen bij voorkeur op papier te staan. Wanneer bij een longbloeding direct midazolam gegeven wordt, kan het de patiënt bespaard blijven een afschuwelijke dood bewust mee te maken. Het is handig om midazolam in huis achter te laten, zodat het in geval van nood direct voorhanden is als iemand (huisarts, wijkverpleegkundige) op tijd aanwezig is om deze medicatie toe te dienen.
Anamnese en onderzoek
Kennis over de wijze waarop de onderliggende ziekte zich in de regel ontwikkelt, draagt bij aan het achterhalen van de oorzaak. Huisartsen weten meestal wel dat dyspnoe vaak voorkomt bij longcarcinoom en de complicaties daarvan. Bij mammacarcinoom is dat wat minder bekend. Niet alleen de uitbreiding van de ziekte naar de longen kan dyspnoe veroorzaken (lokale metastase, lymfangitis, pleuritis of pericarditis), maar ook de ontwikkeling van levermetastasen en ascites. De ernst van de dyspnoe en het tempo waarin deze zich ontwikkelt, kunnen extra informatie opleveren over de achterliggende oorzaak: een zeer snel ontstane totale obstructie (bloeding in de tumor) en een grote bloeding geven acuut heftige klachten. Pleuravocht, pneumonie, anemie en ascites ontstaan langzamer, waardoor de dyspnoe geleidelijker toeneemt en aanvankelijk als minder ernstig wordt ervaren. Bij multipele longembolieën neemt de dyspnoe vaak snel toe. Bij lymfangitis carcinomatosa heeft de patiënt vaak prikkelhoest naast de dyspnoe. Pericarditis carcinomatosa geeft behalve dyspnoe nogal eens klachten van pijn op de borst, duizeligheid en hoesten. Hemoptoë moet gedifferentieerd worden van haematemesis en nasofaryngeale bloedingen. Meestal hoest de patiënt bij hemoptoë. Het bloed is licht rood en nogal eens vermengd met slijm. De mate van dyspnoe is, op dezelfde wijze als bij pijn, vast te stellen en te vervolgen met een visueel-analoge schaal. Na een algemeen lichamelijk onderzoek, onder meer gericht op symptomen als vermoeidheid, bleekheid, oedeem en cyanose, kijkt men gerichter naar verschijnselen die passen bij een van de specifiek beschreven oorzaken. Bij een patiënt met een toenemende obstructie in de luchtwegen kan men een inspiratoire stridor of inspiratoir piepen horen. Bij uitgebreide tumorgroei in de longen of afsluiting van een hoofdbronchus is er verminderd tot afwezig ademgeruis. In het laatste geval is er bij auscultatie een links-rechtsverschil te horen, terwijl één thoraxhelft zichtbaar kan achterblijven bij ademen. Bij het VCS-syndroom zijn de ernst en uitbreiding van de verschijnselen afhankelijk van de lokalisatie, het tempo van ontstaan en de mate van bloedstroombelemmering. Vaak heeft de patiënt een gestuwd hoofd, uitgezette venen in de hals en op de borst, cyanose en hoofdpijn. Bij pleuravocht is er demping te horen en is er sprake van opgeheven ademgeruis. Bij lymfangitis carcinomatosa zijn, net als bij multipele longembolieën, bij fysisch-diagnostisch onderzoek geen duidelijke afwijkingen te vinden. Bij pericarditis carcinomatosa is er veneuze stuwing en een pulsus paradoxus. In een aantal gevallen is het moeilijk door middel van anamnese en lichamelijke onderzoek alléén de juiste oorzaak te achterhalen. Aanvullend onderzoek zoals echografie en röntgenonderzoek kunnen behulpzaam zijn om een vermoeden van een oorzaak te bevestigen (dreigende obstructie, pleuravocht) of om tot een diagnose te komen wanneer de interpretatie van de bevindingen moeilijk is (embolie, lymfangitis carcinomatosa). Dit onderzoek wordt gedaan in overleg met de specialist en meestal alleen wanneer het therapeutische consequenties heeft.
Behandeling
Algemeen
De meeste oncologische patiënten met dyspnoe hebben een aandoening die een snel beloop kent (longcarcinoom) of waarbij de ziekte zich al in een ver gevorderd stadium bevindt. De dyspnoe en de beleving daarvan staan sterk op de voorgrond. De patiënt is bezig afscheid te nemen van het leven en van zijn naasten. Hij bereidt zich voor op een snel naderende dood. De begeleiding van deze patiënten vraagt om een brede aanpak gericht op de lichamelijke problemen en op psychische, sociale en spirituele aspecten. Wanneer men een (waarschijnlijkheids)diagnose heeft gesteld, kijkt men allereerst of de onderliggende oorzaken zo veel mogelijk weg te nemen zijn. Als dat niet kan, probeert men de dyspnoe te verlichten door middel van een symptomatische aanpak. Steeds zijn de conditie, de prognose en de wens van de patiënt bepalend bij het vaststellen van het beleid. Acute aanvallen van benauwdheid gaan gepaard met paniek, angst en het gevoel dood te gaan. Als in de terminale fase ook de chronische benauwdheid toeneemt, speelt angst een nog grotere rol. 9 Naast maatregelen om de dyspnoe te verlichten is de patiënt gebaat bij aandacht voor de angst. Veel patiënten zijn bang om te stikken. De kans hierop is gelukkig zeer klein. De angst neemt vaak aanzienlijk af als de patiënt en zijn naasten voldoende ruimte krijgen om vragen te stellen over de ziekte en informatie krijgen over hetgeen hen mogelijk te wachten staat.
Causale behandeling
Veel causale palliatieve behandelingen kunnen alleen in het ziekenhuis plaatsvinden. Goede kennis hierover maakt het voor huisarts en patiënt gemakkelijker voor- en nadelen tegen elkaar af te wegen. Uit ervaring blijkt dat niet alle specialisten voldoende op de hoogte zijn van bestaande mogelijkheden en nieuwe ontwikkelingen, zodat een kritische houding van de huisarts nodig blijft. In sommige gevallen kunnen deze behandelingen een verbetering van de kwaliteit van leven geven, zoals bij een (dreigende) obstructie van de trachea of een bronchus en bij het VCS-syndroom. In het eerste geval zijn er verschillende behandelopties: chemotherapie, externe radiotherapie, lasertherapie, brachytherapie (lokale radiotherapie) en plaatsen van een stent in het geval van compressie van buitenaf. Bij het VCS-syndroom heeft endovasculaire stentplaatsing de voorkeur. Bij 95% van de patiënten neemt op korte termijn de obstructie af waardoor de klachten verminderen, onafhankelijk van de oorzaak van de obstructie. 10 Bij (dreigende) obstructie en het VCS-syndroom geeft men daarnaast corticosteroïden met als doel de oedeemcomponent te doen afnemen. De keuze om een longembolie wel of niet te behandelen met anticoagulantia is niet eenvoudig. Patiënten met kanker, en zeker met longkanker, hebben op zich al een grote kans op een bloeding. Heeft een patiënt veel klachten, dan zal de prognose bepalend zijn bij het besluit om causaal te behandelen en daarbij de kans te lopen op een bloeding, of te kiezen voor symptomatische behandeling. Als het mogelijk is pleuravocht te verwijderen, heeft een patiënt daar over het algemeen baat bij. Wanneer het vocht snel terugkomt, is pleurodese te overwegen. Tegenwoordig is het mogelijk een drain in situ te laten, waarbij de patiënt bij toegenomen klachten zelf vocht kan verwijderen. Soms wordt voor deze indicatie chemotherapie gegeven. Pericardvocht kan gepuncteerd worden. Vooral bij een harttamponnade is snel ingrijpen gewenst. Er zijn meerdere mogelijkheden om kleinere bloedingen te behandelen zoals radiotherapie, lasertherapie en elektrocauterisatie. Nogmaals benadrukken we hier het belang van een zorgvuldige afweging van de verschillende behandelmogelijkheden. Deze keuze hangt in grote mate af van de wensen en de prognose van de patiënt. Een ascitespunctie kan de huisarts zelf doen. Het verwijderen van enkele liters ascitesvocht geeft vaak een enorme verlichting van de dyspnoe. Behandeling van factoren die niet ten grondslag liggen aan het specifieke oncologische probleem of die meer algemeen van aard zijn, draagt eraan bij de dyspnoe te verminderen. Veel ouderen hebben behalve kanker ook COPD of hartfalen. Hiervoor zijn veel therapeutische opties. Bronchospasme treedt ook bijna altijd op bij longkanker, zodat hier een indicatie is voor bronchusverwijders en/of corticosteroïden. Bij een (forse) anemie is het geven van een bloedtransfusie te overwegen.
Symptomatische behandeling
Niet-medicamenteus
De niet-medicamenteuze behandeling van patiënten met dyspnoe is erop gericht de betekenis van de benauwdheid te exploreren en uitleg te geven over de aandoening en het te verwachten beloop. Ontspanningsoefeningen en afleiding dragen ertoe bij dat patiënten de dyspnoe beter kunnen accepteren en ermee om kunnen gaan. De omgeving wordt zo veel mogelijk betrokken bij deze begeleiding. Naasten kunnen bijvoorbeeld de schouders van de patiënt masseren, zodat hij meer ontspant. Er is veel te bereiken met een rustige benadering, juist omdat de angst zo'n grote rol speelt bij de patiënt en zijn naasten. Nabijheid van vertrouwde personen kan de patiënt steun geven wanneer de dyspnoe op momenten hevig toeneemt en paniek ontstaat. Mevrouw Vrede kroop bijna weg in de armen van haar naasten als zich zo'n situatie voordeed. Zij voelde zich door hen beschermd. Uit onderzoek onder patiënten met longkanker bleek dat intensieve begeleiding zinvol is. De patiënten die psychologische ondersteuning kregen, leerden hun ademhaling te reguleren, zich te ontspannen en hun bezigheden goed in te delen. Zij waren minder benauwd dan patiënten in de controlegroep die deze begeleiding niet kregen. 11 In de thuissituatie kunnen verpleegkundigen en fysiotherapeuten een belangrijke rol spelen in deze begeleiding. Soms ervaren patiënten verlichting van de dyspnoe wanneer zij bij een open raam zitten of wanneer een ventilator aanstaat. Hieraan zou ten grondslag liggen dat receptoren in het gelaat, wanneer zij geprikkeld worden, invloed hebben op het gevoel van dyspnoe. 12
Zuurstof
In de inleiding hebben wij beschreven dat benauwdheid niet alleen voor de patiënt, maar ook voor de naasten een beangstigende ervaring is. Dyspnoe is, ondanks adequate maatregelen, niet altijd afdoende te verlichten. Praktisch iedereen weet dat het mogelijk is zuurstof te geven aan patiënten. Zuurstof geven betekent iets doen, zodat het machteloze gevoel er met lege handen bij te staan, afneemt. Zuurstof wordt ook in de thuissituatie regelmatig gegeven. Soms op goede indicatie, bijvoorbeeld bij de groep patiënten met COPD, maar bij oncologische patiënten nogal eens op niet zo duidelijke gronden. De behandelend arts maakt dan de inschatting dat zuurstof verlichting van de klachten geeft. Bovendien kan het voor de omgeving een zekere rust geven. Dit beleid is zeker te verdedigen. Booth et al. keken naar het effect van het gebruik van zuurstof bij patiënten met COPD, hartfalen en kanker. 13 Hun conclusie is dat zuurstof een bewezen meerwaarde kan hebben bij het verlichten van dyspnoe bij een geselecteerde groep patiënten met een voortgeschreden oncologische aandoening of met COPD. Bij de individuele oncologische patiënt is echter niet te voorspellen of de toediening van zuurstof effect zal hebben: er zijn geen parameters voorhanden die helpen de juiste patiënten hiervoor te selecteren. Patiënten met kanker hebben in 40% van de gevallen een hypoxemie. Maar lang niet al deze patiënten zijn benauwd en niet iedereen met dyspnoe heeft een tekort aan zuurstof in het bloed. 14 Men moet dus niet afgaan op bijvoorbeeld een pols-oximeter, maar op de eigen ‘klinische blik’ en vooral aan de patiënt vragen of de toegediende zuurstof helpt de kwaliteit van leven te verbeteren. Zuurstofgebruik heeft ook nadelen. De kans bestaat dat de zuurstof een overheersende rol gaat spelen: patiënt en familie zijn dan bijna psychisch afhankelijk van de zuurstoffles. Zelfs in de stervensfase is het in zo'n geval lastig te stoppen met de toediening ervan. Het gebruik van zuurstof beperkt iemands activiteiten. Er bestaat gevaar voor brandwonden in het gezicht wanneer de patiënt zou gaan roken. Zuurstoftoediening is ten slotte ook duur.
Medicamenteus
Morfine is het meest effectieve geneesmiddel bij de symptomatische behandeling van dyspnoe. 15 Het kan zowel oraal als subcutaan worden toegediend en heeft geen negatief effect op de longfunctie. 16 Over de toedieningsvorm en dosering bij aanvang zijn geen eensluidende adviezen te vinden. Sommigen adviseren met een kortwerkend preparaat te beginnen, anderen menen dat ook een langwerkend middel voldoet. De aanbevolen aanvangsdosering is meestal 5 mg, terwijl een dosering van 2,5 mg morfine soms ook al verlichting geeft. Ten slotte zijn er ook ten aanzien van toediening op een ‘zo nodig’-basis of in een regelmatig schema nog geen eenduidige adviezen. 8 Wel is voor de dosering van belang of de patiënt al opioïden gebruikt. De conclusie is dat een patiënt die nog geen opioïden gebruikt in een niet-acute situatie tweemaal daags 10 mg langwerkend morfine kan krijgen, of 2,5-10 mg kortwerkend morfine oraal of subcutaan elke 4 uur. De dosering wordt dan verder opgehoogd op geleide van de klachten. De kortwerkende morfine kan omgezet worden naar een langwerkend preparaat wanneer de toestand van de patiënt weer stabiel is. Bij patiënten die al morfine gebruiken, verhoogt men de dosering van de morfine met 25-50% om de dyspnoe te bestrijden. Het vernevelen van mucolytica en/of luchtwegverwijders (salbutamol bijvoorbeeld) met fysiologisch zout is zinvol bij benauwde patiënten. 17 Van verneveling van morfine is nog niet duidelijk aangetoond dat dit beter werkt dan verneveling met fysiologisch zout. 18 Bij angstige patiënten geeft men anxiolytica, zoals oxazepam, lorazepam of midazolam, op geleide van de klachten. Zowel de anxiolytische als de sederende werking vermindert de dyspnoe. Nogal eens wordt bij de medicamenteuze behandeling van dyspnoe een anxiolyticum standaard naast morfine gegeven: patiënten die ernstig benauwd zijn, zijn immers eigenlijk ook altijd ook bang.
Longbloeding
Een fatale longbloeding is voor de patiënt en de omstanders zeer ingrijpend. Dit geldt ook voor de huisarts die zo'n gebeurtenis meemaakt. Het komt (gelukkig) slechts bij 3% van de patiënten met longkanker voor. Ongeveer de helft van de patiënten met longkanker hoest of geeft bloed op in de palliatieve fase. Bij elk van hen zou dit in principe een voorbode kunnen zijn van een massale bloeding. Helaas is niet te voorspellen welke patiënt een grote bloeding zal krijgen en welke niet. Dit stelt de huisarts voor een dilemma: bespreek ik de kans op een bloeding die zich waarschijnlijk nooit zal voordoen of bespaar ik patiënt en familie het vooruitzicht op zo'n angstig scenario? Het bespreken van de kans op een bloeding kan angst en onrust veroorzaken. Aan de andere kant zullen patiënten zich bij het opgeven van bloed vaak al afvragen of zij misschien in hun bloed zullen stikken. Wanneer de huisarts deze angst en de mogelijkheden die er zijn om ernstig lijden door een bloeding te verlichten met de patiënt bespreekt, kan dit de angst doen afnemen. Tegelijkertijd kunnen naasten de suggestie krijgen in zo'n geval donkere handdoeken te gebruiken om het bloed op te vangen en liefst naast of achter de patiënt te gaan staan of zitten: de gebeurtenis op zich maakt al een onuitwisbare indruk. Wanneer een dergelijke bloeding zich voordoet, is er maar een kleine kans dat de huisarts ter plaatse is voordat de patiënt overleden is. Soms is hij wel op tijd, of is er een verpleegkundige in huis om de patiënt direct 15-30 mg midazolam toe te dienen zodat hij buiten bewustzijn raakt. 16 Intraveneuze toediening heeft hierbij de voorkeur, maar is – alleen al door de onrust van de patiënt – lang niet altijd mogelijk. De injectie wordt dan hoog in de bovenarm diep intramusculair – desnoods door de pyjama heen – of subcutaan gegeven.
Ten slotte
De begeleiding van patiënten met ziektebeelden waarbij dyspnoe in de laatste fase regelmatig voorkomt, is nu al een belangrijke taak van de huisarts. Het aantal patiënten hiermee zal in de toekomst flink toenemen. Dyspnoe wordt vaak als zeer beangstigend en direct levensbedreigend ervaren door de patiënt, door zijn naasten en ook nogal eens door hulpverleners. Objectieve parameters voor de mate van dyspnoe zijn er niet. Anamnese en lichamelijk onderzoek alleen geven niet altijd voldoende uitsluitsel over de onderliggende oorzaak. Door met de behandelend specialist te overleggen kan de huisarts voor de individuele patiënt het beste beleid bepalen. Oorzakelijke behandelingen kunnen de kwaliteit van leven sterk verbeteren en vinden meestal plaats in het ziekenhuis. Wanneer hiervoor geen mogelijkheden meer zijn, ondersteunt de huisarts de patiënt en zijn naasten door de dyspnoe zo goed mogelijk te verlichten en zorg te hebben voor de gevolgen en beleving hiervan. Wijkverpleegkundige en fysiotherapeut kunnen aan dit proces een waardevolle bijdrage leveren.
Literatuur
- 1.Nordgren L, Sorensen S. Symptoms experienced in the last six months of life in patients with end-stage heart failure. Eur J Cardiovasc Nurs 2003;2:213-7.
- 2.Voltz R, Borasio GD. Palliative therapy in the terminal stage of neurological disease. J Neurol 1997;244(Suppl 4):S2-S10.
- 3.Dudgeon DJ, Kristjanson L, Sloan JA, Lertzman M, Clement K. Dyspnea in cancer patients: prevalence and associated factors. J Pain Symptom Manage 2001;21:95-102.
- 4.Murray CJL, Lopez AD. Alternative projections of mortality and disability by causes 1990-2020. Global burden of disease study. Lancet 1997;349:1498-1504.
- 5.Chan K, Sham MMK, Tse DMW, Berit Thorsen A. Palliative medicine in malignant respiratory diseases. In: Doyle D, Hanks GWC, Cherry NI, Calman KC, editors. Oxford Textbook of Palliative Medicine, 3rd ed. New York: Oxford University Press, 2004.
- 6.Ripamonti C, Fusco F. Respiratory problems in advanced cancer. Support Care Cancer 2002;10:204-16.
- 7.Stretton F, Edmonds P, Marrinan M. Malignant pleural effusions. Eur J Palliat Care 1999;6:5-9.
- 8.Woodruff R. Palliative Medicine. Evidence-based symptomatic and supportive care for patients with advanced cancer. 4th ed. Melbourne: Oxford University Press, 2004.
- 9.Odriscoll M, Corner B, Bailey C. The experience of breathlessness in lung cancer. Eur J Cancer Care 1999:37-43.
- 10.Rowell NP, Gleeson FV. Steroids, radiotherapy, chemotherapy and stents for superior vena caval obstruction in carcinoma of the bronchus. Cochrane database Syst Rev 2001;(4); CD001316.
- 11.Bredin M, Corner J, Krishnasamy M, Plant H, Bailey C, A’ Hern R. Multicentre randomised controlled trial of nursing intervention for breathlessness in patients with lung cancer. BMJ 1999;318:901-4.
- 12.Schwartzstein RM, Lahive K, Pope A, Weinberger SE, Weiss JW. Cold facial stimulation reduces breathlessness induced in normal subjects. Am Rev Respir Dis 1987;136:58-61.
- 13.Booth S, Anderson H, Swannick M, Wade R, Kite S, Johnson M. The use of oxygen in the palliation of breathlessness. A report of the expert working group of the scientific committee of the association of palliative medicine. Respir Med 2004;98:66-77.
- 14.Wymenga ANM, Van der Werf TS, Sleijfer DTH. Dyspnoe bij kankerpatiënten; oorzaken en therapie. Ned Tijdschr Palliat Zorg 2003;4:49-54.
- 15.Jennings AL, Davies AN, Higgins JP, Broadley K. Opioids for the palliation of breathlessness in terminal illness. Cochrane Database Syst Rev 2001;(4); CD002066.
- 16.Mazzocato C, Buclin T, Rapin CH. The effects of morphine on dyspnea and ventilatory function in elderly patients with advanced cancer: a randomized double-blind controlled trial. Annals of Oncol 1999;10:1511-14.
- 17.De Graeff A, Verhagen EH, Eliel MR, Hesselman GM, Kroeze-Hoogendoorn GJ. Oncologieboek deel II, Richtlijnen Palliatieve Zorg. Utrecht: IKMN, 2002.
- 18. A systematic review of the use of opioids in the management of dyspnoea. Thorax 2002;57:939-44.
Reacties
Er zijn nog geen reacties.